宫颈癌适应症,原本不在机构研报推算的PD-1预期销售额之内。
全球每年新增宫颈癌超过57万例,死亡病例超过31万例。其中,复发性难治性宫颈癌预后不良,5年总生存率(OS)仅为17%。
根据GLOBOCAN2020统计数据,中国🇨🇳每年新增病例10.6万例,每年死亡4.8万例。
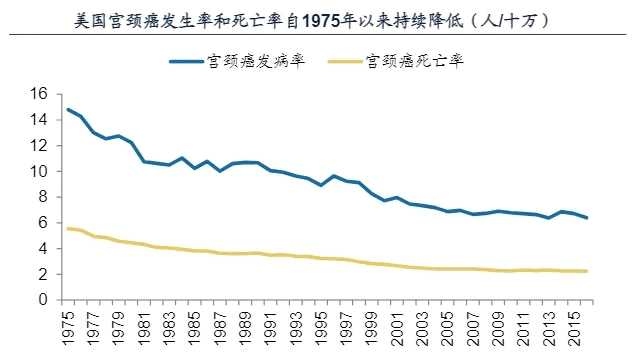
宫颈癌在美国🇺🇸也是大病种。每年新增6+万例,每年死亡3+万例。
2014年,美国FDA批准贝伐珠单抗用于复发性难治性宫颈癌的一线治疗。
2018年6月,美国FDA批准K药用于复发难治性宫颈癌(PD-L1表达水平>1%)二线治疗,这两种药物均为国外研发。
康方生物-B(09926)PD-1/CTLA-4双抗(AK104)获得了美国🇺🇸FDA快速审批通道资格(FTD)。
康方生物在公告中称,有快速审批通道资格的候选药物,可有资格(进一步)与FDA进行更频繁的沟通、优先评审(如果符合相关标准)及新药申请(NDA)的滚动评审,加快相关药物的开发及上市进程。
例如,君实生物-U(SH688180)PD-1(特瑞普利单抗)鼻咽癌≥2线治疗在美国🇺🇸注册上市就是滚动审评。

迄今为止,中国🇨🇳CDE授予了三家中国药企在宫颈癌适应症的突破性疗法认定☆,
①恒瑞医药(SH600276)PD-1联合法米替尼,一线治疗宫颈癌。目前为止,正在开展一线治疗3期临床。
②康方生物PD-1/CTLA-4双抗,二线治疗宫颈癌。目前为止,联合化疗±贝伐珠单抗,正在开展一线治疗3期临床。
③
另外,正大天晴的PD-L1正在开展宫颈癌二线治疗2期临床。
此外,
Balstilimab与Zalifrelimab
具体临床试验数据不错,单药balstilimab二线治疗宫颈癌入组160人的ORR为14%;与zalifrelimab联合二线治疗入组143人的ORR为22%。
并且对于PD-L1表达<1%的患者也部分有效。

宫颈癌的免疫治疗进展非常迅速。
从
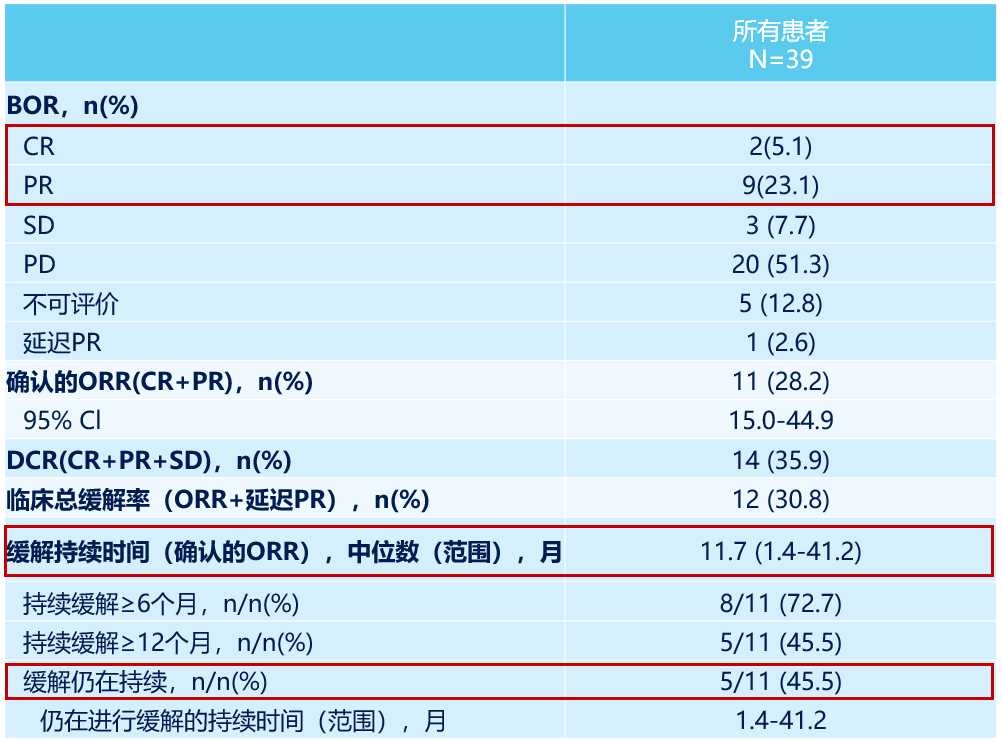
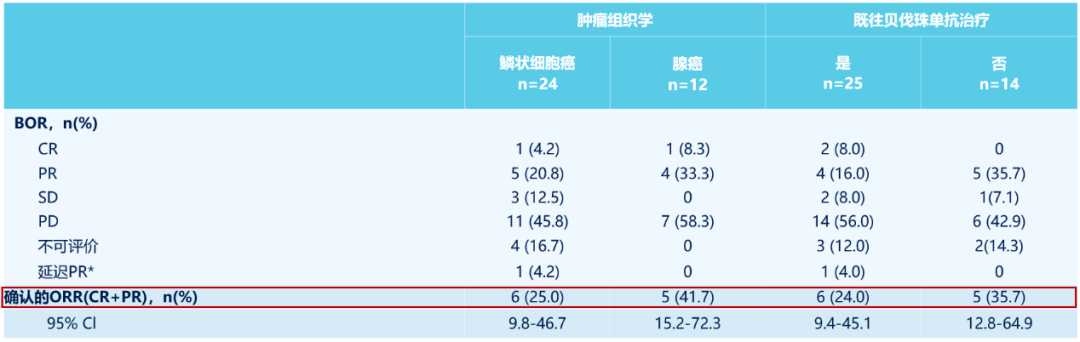
上述研究入组了30.8%的宫颈腺癌患者,真实世界中宫颈鳞癌比例为75%,宫颈腺癌患者比例为20%。宫颈腺癌预后较差,治疗起来更困难。而M7824在这部分腺癌患者中的ORR达到了41.7%,无疑是突破性疗效。
目前为止,
PD-1单抗或者双抗的宫颈癌适应症市场前景?
(一)假设PD-1单抗每年费用为3万元,一线治疗渗透率为80%,响应率为46%,二线治疗渗透率为80%,响应率为40%。
中国PD-1单抗的宫颈癌适应症市场规模=(10.6万*80%*46%*12个月*3万元)+(4.8万*80%*40%*6个月*1.5万元)=11.70亿元+2.3亿元=14亿元。
(二)假设PD-1/XXX双抗每年费用为12万元,一线治疗渗透率为80%,响应率为46%,二线治疗渗透率为80%,响应率为40%。
中国PD-1/XXX双抗的宫颈癌适应症市场规模=(10.6万*80%*46%*12个月*12万元)+(4.8万*80%*40%*6个月*3万元)=46.8亿元+9.2亿元=56亿元。
综上所述,宫颈癌适应症成为PD-1/XXX双抗的广阔市场前景。