2021年,君实生物(01877)PD-1联合阿昔替尼vs默沙东(MRK)K药单药,头对头对照试验,一线治疗晚期黏膜黑色素,全球多中心3期临床已经启动。
与K药的头对头对照试验,展现了君实生物PD-1在黑色素瘤适应症上的全球野心。
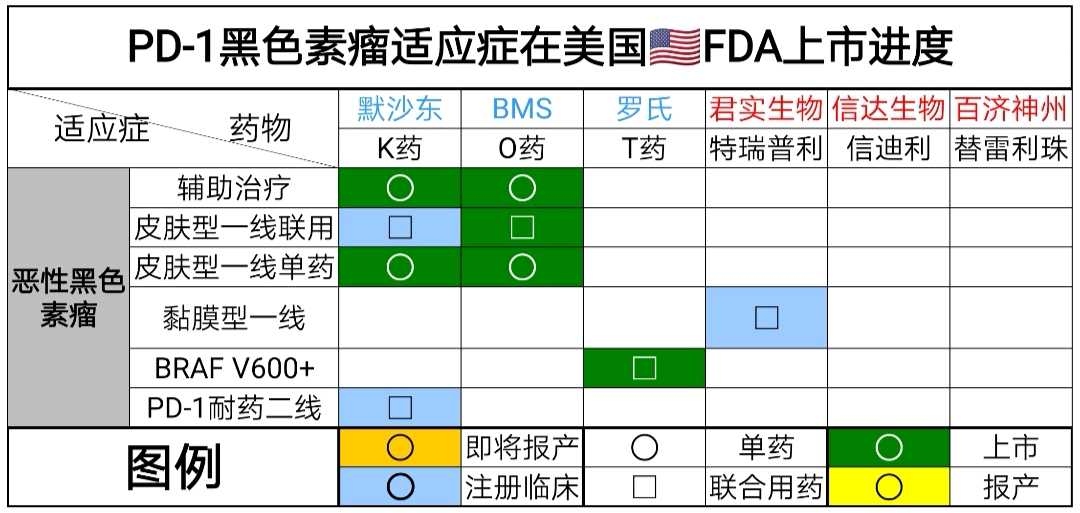
PD-1的黑色素瘤适应症每年全球市场规模>80亿美元(500亿元RMB)。
下图是两个独立的单臂注册临床试验研究,研究人群均为中国黑色素瘤患者。
类似的研究方案,将结果进行横向参考:尽管君实生物特瑞普利单抗(PD-1)入组了更多后线治疗的病人,入组了更多的黏膜黑色素瘤。特瑞普利单抗仍然取得了更长的mPFS=3.6个月,更长的OS 23.2个月。

另外,君实生物-U(SH688180)PD-1联合阿昔替尼一线治疗晚期黏膜黑色素瘤,获得了美国🇺🇸FDA快速通道资格。意味着PFS可以作为在FDA获批上市。
2019年8月12日,君实生物特瑞普利单抗(PD-1)联合阿昔替尼治疗晚期黑色素瘤的2期临床结果发表在《临床肿瘤学杂志》(JournalofClinicalOncology)上,研究结果显示:特瑞普利单抗联合阿昔替尼治疗未接受过化疗的晚期黏膜黑色素瘤患者可获得48.3%客观缓解率(ORR),及86.2%的疾病控制率(DCR),中位无进展生存期(mPFS)达到了7.5个月。
预计2022年底,就可以PFS数据读出,达到主要临床终点。
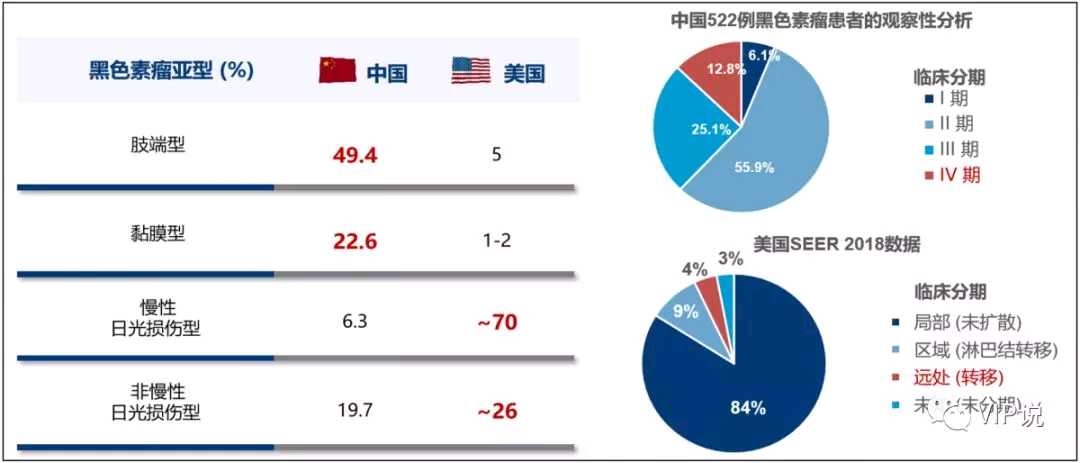
由于中国🇨🇳和美国🇺🇸在黑色素瘤的亚型上,有显著不同比例,中国🇨🇳的黏膜型和肢端型比例高达70%,而美国🇺🇸的皮肤型黑色素瘤比例高达90%。
目前普遍认为
2018年,君实生物PD-1已经在中国开展晚期黑色素单药一线治疗3期临床。
展开阅读全文
赞 | 0
收藏
分享
观点区
请先 登录 后发表观点~